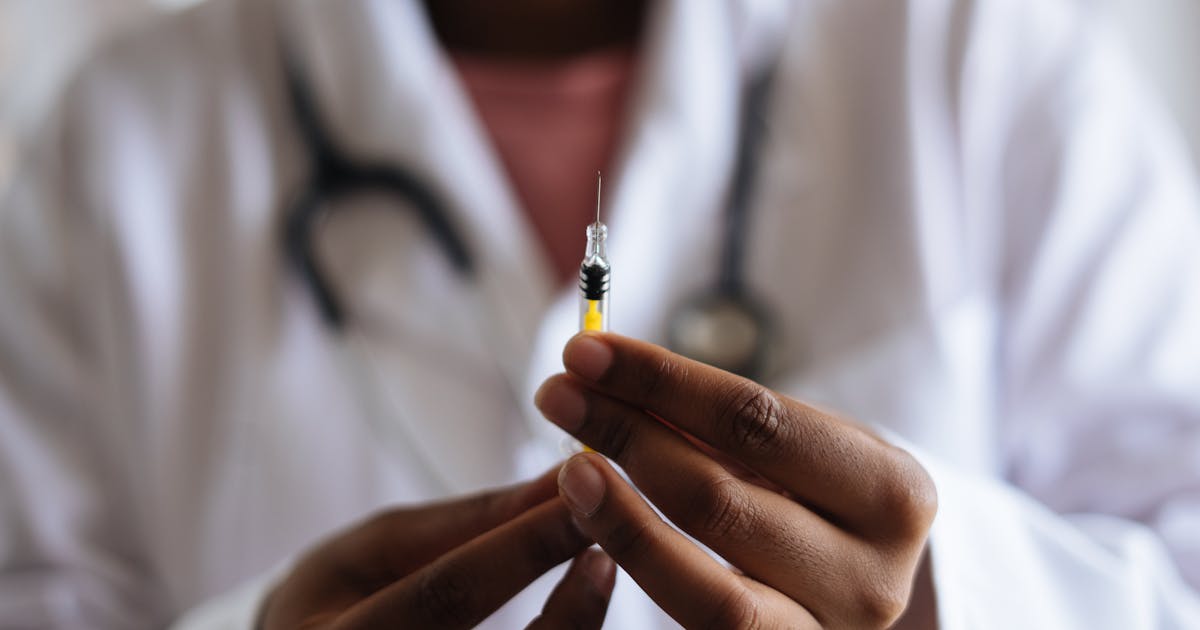
I 2026 tar medisinen et historisk steg: vaksiner basert på budbringer-RNA (mRNA) brukes ikke lenger bare til å forebygge infeksjoner. De angriper nå også kreft, med resultater som fortsatt var utenkelige for fem år siden. BioNTech, Moderna og flere europeiske universitetsmiljøer melder om kliniske studier med lovende — til og med spektakulære — resultater. Her er det du bør vite.
Hvordan fungerer en mRNA-vaksine mot kreft?
I motsetning til klassiske forebyggende vaksiner har terapeutiske kreftvaksiner ikke som mål å hindre at en sykdom oppstår: de gis etter diagnosen, for å mobilisere pasientens immunsystem mot egne tumorceller.
Prinsippet bygger på mRNA-teknologien: Pasienten får injisert en sekvens av budbringer-RNA som koder for antigener som er spesifikke for svulsten — proteiner kalt neoantigener, som stammer fra mutasjoner som er særegne for pasientens kreft. Immunsystemet lærer å gjenkjenne disse markørene og målrette angrep mot cellene som bærer dem.
Hver vaksine er derfor personlig tilpasset: Den lages i løpet av noen uker ut fra en tumorbiopsi og er helt tilpasset den genomiske profilen til pasientens svulst. Det er her hele revolusjonen ligger.
Resultatene som skaper overskrifter i 2026
BioNTech og vaksinen med 88 % effekt
Det tyske selskapet BioNTech — medutvikler av Pfizer-BioNTech-vaksinen mot Covid-19 — sikter mot kommersialisering av en første kreftbehandling i 2026. Studiene på enkelte hudkrefttyper (melanom) viser en oppsiktsvekkende effekt: 88 % reduksjon i risikoen for tilbakefall kombinert med immunterapi med pembrolizumab. Disse tallene, presentert på ASCO (American Society of Clinical Oncology), har sendt sjokkbølger gjennom det medisinske miljøet.
Vaksinen mot bukspyttkjertelkreft gir håp
Bukspyttkjertelkreft er en av de mest fryktede kreftformene: Femårs overlevelse overstiger sjelden 10 %. I 2026 viser resultater presentert på konferansen til American Association for Cancer Research at blant pasientene som utviklet en immunrespons på den personlige mRNA-vaksinen, var 87,5 % fortsatt i live seks år etter behandlingsstart. Det regnes som et bemerkelsesverdig resultat for denne sykdommen.
Pfizer-prisen 2026 belønner et team fra Genève
Universitetssykehuset i Genève (HUG) og Universitetet i Genève mottok Pfizer-prisen 2026 for sin terapeutiske vaksine MVX-ONCO-1. I studien deres viste mer enn halvparten av pasientene en klinisk gevinst — fra stabilisering av sykdommen til betydelig forlenget overlevelse. Det er et sterkt signal som bekrefter levedyktigheten til disse personlige immunologiske tilnærmingene.
Hvorfor 2026 er et skjebneår
Flere faktorer møtes og gjør 2026 til et vendepunkt:
- Produksjonstidene har falt: Å produsere en personlig mRNA-vaksine tar nå mindre enn seks uker, mot flere måneder tidligere. Logistikken blir bedre og kostnadene faller.
- Regulatorene øker tempoet: Amerikanske FDA og europeiske EMA har innført hurtigspor for godkjenning av innovative terapier mot kreftformer med dårlig prognose.
- Studiene blir stadig flere: Mer enn 200 kliniske studier med mRNA-vaksiner mot kreft pågår i verden. Melanom, lunge, tykktarm, bukspyttkjertel, bryst — nesten alle typer svulster er berørt.
- Synergiene med immunterapi: Kombinert med sjekkpunkthemmere mangedobler mRNA-vaksiner aktiveringen av cytotoksiske T-lymfocytter — cellene som dreper kreft.
Hvilke kreftformer prioriteres?
Ikke alle kreftformer responderer likt på disse vaksinene. Såkalte immunogene svulster — de som har mange mutasjoner og dermed mange neoantigener — er de beste kandidatene. Dette gjelder melanom, ikke-småcellet lungekreft, kolorektal kreft med mikrosatellittinstabilitet, og i en viss grad blære- og nyrekreft.
Derimot er såkalte “kalde” kreftformer — som naturlig unngår immunsystemet — fortsatt en utfordring. Det forskes på å “varme dem opp” før vaksinen injiseres, særlig gjennom korte kjemoterapier eller målrettede behandlinger på forhånd.
Hva med bivirkningene?
En av de store fordelene med terapeutiske mRNA-vaksiner er toleranseprofilen. I motsetning til tradisjonell kjemoterapi ødelegger de ikke friske celler vilkårlig. De observerte bivirkningene er hovedsakelig lokale reaksjoner på injeksjonsstedet (rødhet, hevelse), forbigående tretthet og noen ganger lett feber — typiske effekter av immunstimulering.
Mer alvorlige autoimmune effekter er observert i et mindretall av tilfellene, men de er fortsatt sjeldne og som regel håndterbare, særlig når vaksinen brukes uten tilknyttet immunterapi.
Når blir disse behandlingene tilgjengelige i Frankrike?
BioNTech planlegger å sende inn en søknad om markedsføringstillatelse til EMA for sin vaksine mot melanom innen utgangen av 2026. Hvis godkjenningen gis innen vanlige frister (12 til 18 måneder), kan de første franske pasientene få tilgang i løpet av 2027 eller 2028, først gjennom programmer for tidlig tilgang (ATU i Frankrike).
For andre kreftformer blir tidshorisonten lengre: Fase III-studier pågår fortsatt for de fleste av dem. Men dynamikken er tydelig, og ekspertene er enige: mRNA-vaksiner mot kreft er ikke lenger science fiction. De går inn i presisjonsmedisinens tidsalder.
«Vi står ved begynnelsen av en ny terapeutisk æra. Budbringer-RNA vil forandre onkologien slik det har forandret vaksinevitenskapen.» — Ugur Sahin, administrerende direktør i BioNTech
Dette bør du huske
mRNA-vaksiner mot kreft representerer et av de mest betydelige medisinske fremskrittene siden immunterapien. I 2026 hoper de kliniske bevisene seg opp, regulatorene tilpasser seg, og industrien øker tempoet. Hvis du eller en av dine nærmeste er berørt av en kreftdiagnose, bør du snakke med onkologen din: Enkelte kliniske studier er åpne for rekruttering, og franske medisinske team er stadig mer aktive i disse innovative protokollene.
Krigen mot kreft går inn i en ny fase. Og for første gang hviler håpet på en teknologi som lærer å lese — og ødelegge — kreft innenfra.

 Norwegian
Norwegian  French
French  English
English  Spanish
Spanish  Chinese
Chinese  Japanese
Japanese  Korean
Korean  Hindi
Hindi  German
German