En fevrier 2025, un nourrisson prenomme KJ est entre dans l'histoire de la medecine. Atteint d'une maladie genetique rare et potentiellement mortelle, il est devenu le tout premier etre humain a recevoir une therapie genique CRISPR entierement personnalisee. Un an plus tard, les resultats depassent les esperances et ouvrent une voie revolutionnaire pour des millions de patients dans le monde.
Une maladie rare aux consequences devastatrices
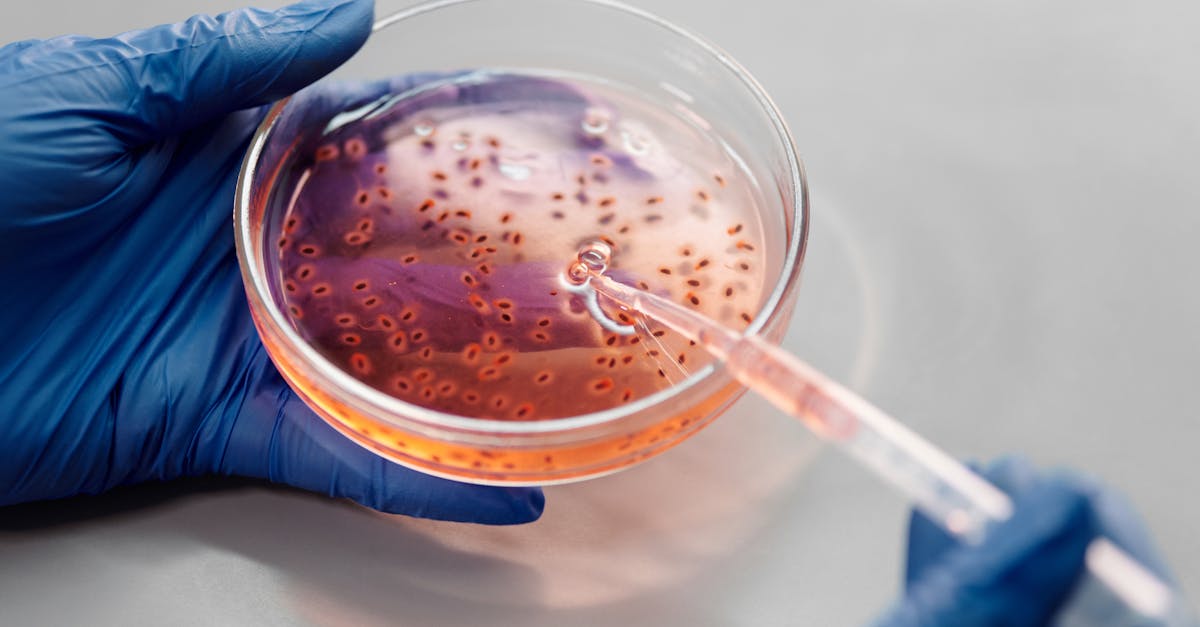
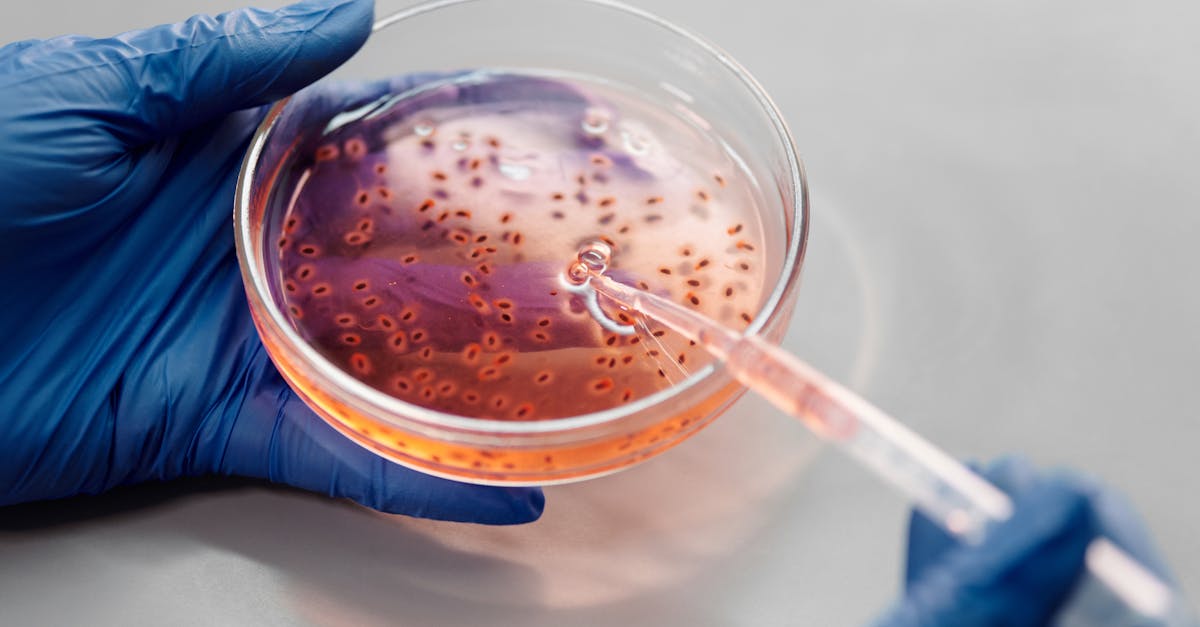
KJ est ne avec un deficit en carbamoyl phosphate synthetase 1 (CPS1), une maladie metabolique hereditaire qui touche environ 1 naissance sur 1,3 million. Cette enzyme, essentielle au cycle de l'uree dans le foie, permet normalement d'eliminer l'ammoniac produit par la degradation des proteines. Sans elle, l'ammoniac s'accumule dans le sang et peut provoquer des lesions cerebrales irreversibles, voire la mort.
Des sa naissance, KJ a du suivre un regime alimentaire extremement pauvre en proteines et prendre de puissants medicaments eliminateurs d'azote pour maintenir des niveaux d'ammoniac supportables. A seulement cinq mois, son etat etait si precaire qu'il a ete inscrit sur la liste d'attente pour une greffe de foie — un acte chirurgical lourd, risque, et dont la disponibilite reste aleatoire pour un si jeune patient.
Six mois pour creer un traitement sur mesure
C'est au Children's Hospital of Philadelphia (CHOP) que l'equipe de la docteure Rebecca Ahrens-Nicklas a releve un defi sans precedent : concevoir, fabriquer et administrer une therapie d'edition genetique personnalisee en seulement six mois. La technologie utilisee, appelee base editing, est une evolution du CRISPR classique. Plutot que de couper l'ADN comme des ciseaux moleculaires, le base editing modifie une seule lettre du code genetique avec une precision chirurgicale, sans provoquer de cassure double brin.
Le traitement a ete encapsule dans des nanoparticules lipidiques — la meme technologie que celle utilisee pour les vaccins ARNm — afin de le delivrer directement aux cellules du foie de KJ. L'objectif : corriger la mutation responsable du dysfonctionnement de l'enzyme CPS1 et restaurer partiellement sa capacite a eliminer l'ammoniac.
Des resultats encourageants un an apres
Le 25 fevrier 2025, KJ a recu sa premiere perfusion. Deux doses supplementaires ont suivi en mars et avril. Comme l'a souligne la docteure Ahrens-Nicklas : "Bien que ce traitement ne soit pas un remede definitif, apres trois perfusions, KJ l'a bien tolere sans effets secondaires graves."
Un an plus tard, les progres sont remarquables. KJ marche, parle, et franchit les etapes de developpement attendues pour son age. Son alimentation a pu etre enrichie en proteines, et les doses de medicaments eliminateurs d'azote ont ete reduites. Meme lors d'episodes de maladie infantile — moments critiques ou l'ammoniac peut monter en fleche — ses niveaux sont restes sous controle.
Une revolution reglementaire pour accelerer l'acces
L'histoire de KJ ne transforme pas seulement la recherche medicale, elle influence aussi la reglementation. Le 23 fevrier 2026, la FDA americaine a annonce un nouveau cadre d'approbation baptise "mecanisme plausible". Ce dispositif permet d'autoriser des therapies personnalisees sur la base de 5 a 10 patients seulement, au lieu des centaines habituellement requis dans les essais cliniques classiques. Une avancee decisive pour les maladies ultra-rares, ou il est parfois impossible de reunir suffisamment de patients pour un essai traditionnel.
L'equipe du CHOP prevoit de soumettre une demande d'essai clinique de phase I/II en 2026 pour une plateforme elargie couvrant plusieurs troubles du cycle de l'uree. Le programme GTIMD (Gene Therapy for Inherited Metabolic Disorders) etudie deja des applications pour les acidemies organiques, les defauts d'oxydation des acides gras et la phenylcetonurie.
Un modele pour la medecine de demain
Ce qui rend le cas de KJ veritablement revolutionnaire, ce n'est pas seulement la therapie elle-meme, mais le modele qu'elle inaugure. Jusqu'ici, developper un medicament prenait en moyenne dix a quinze ans et coutait plusieurs milliards. Ici, un traitement sur mesure a ete cree en six mois pour un seul patient. Si ce processus peut etre industrialise et rendu accessible, c'est toute la medecine des maladies rares qui pourrait etre transformee.
Un scientifique cle de l'equipe ayant traite KJ a d'ailleurs lance en janvier 2026 une startup, Aurora Therapeutics, avec l'ambition de democratiser la production de therapies CRISPR personnalisees. L'objectif : reduire les couts et les delais pour que chaque patient atteint d'une maladie genetique rare puisse un jour beneficier d'un traitement concu specifiquement pour sa mutation.
L'espoir des familles et l'appel a l'action
Les parents de KJ, Kyle et Nicole Muldoon, sont devenus des porte-voix pour la recherche en therapie genique. Nicole a declare : "Les legislateurs peuvent rendre cela possible en investissant dans la recherche et en elargissant l'acces aux soins." Leur temoignage rappelle que derriere les avancees scientifiques, il y a des familles pour qui chaque jour compte.
On estime que plus de 7 000 maladies rares d'origine genetique affectent collectivement entre 300 et 400 millions de personnes dans le monde. Pour la grande majorite d'entre elles, il n'existe aucun traitement specifique. L'approche inauguree avec KJ pourrait, a terme, offrir une lueur d'espoir a chacun de ces patients.
L'histoire de Baby KJ n'est pas seulement une prouesse medicale. C'est le signal que la medecine entre dans une nouvelle ere — celle ou le traitement est concu pour le patient, et non l'inverse. Une revolution silencieuse, lettre par lettre, dans le grand livre de notre ADN.

 Japanese
Japanese  French
French  English
English  Spanish
Spanish  Chinese
Chinese  Korean
Korean  Hindi
Hindi  German
German  Norwegian
Norwegian