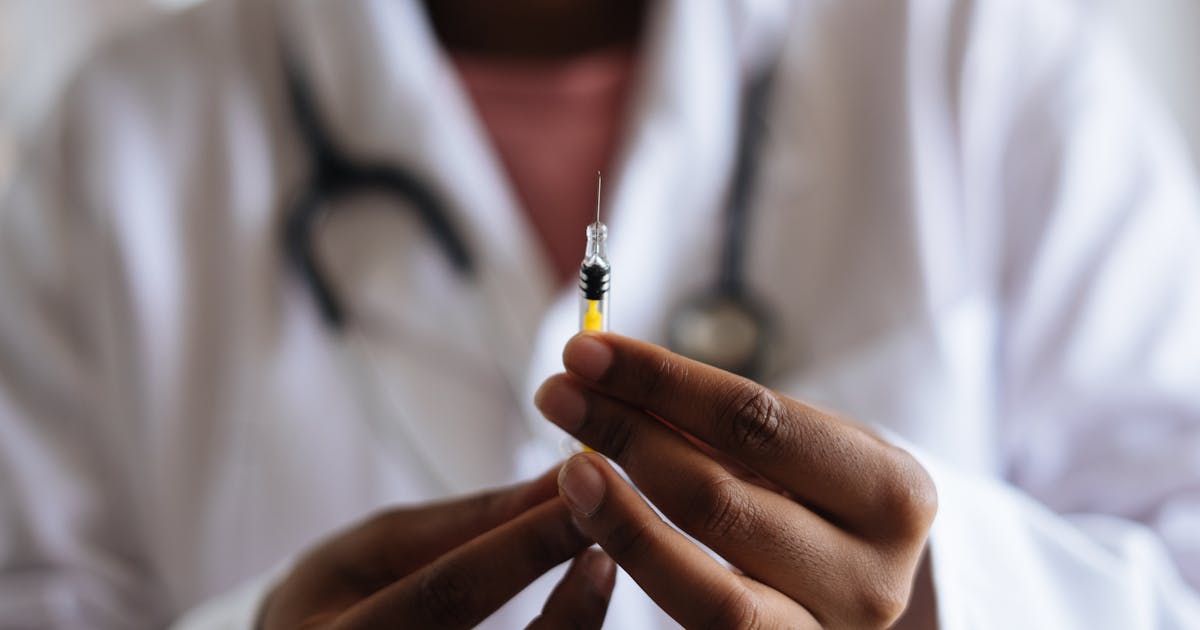
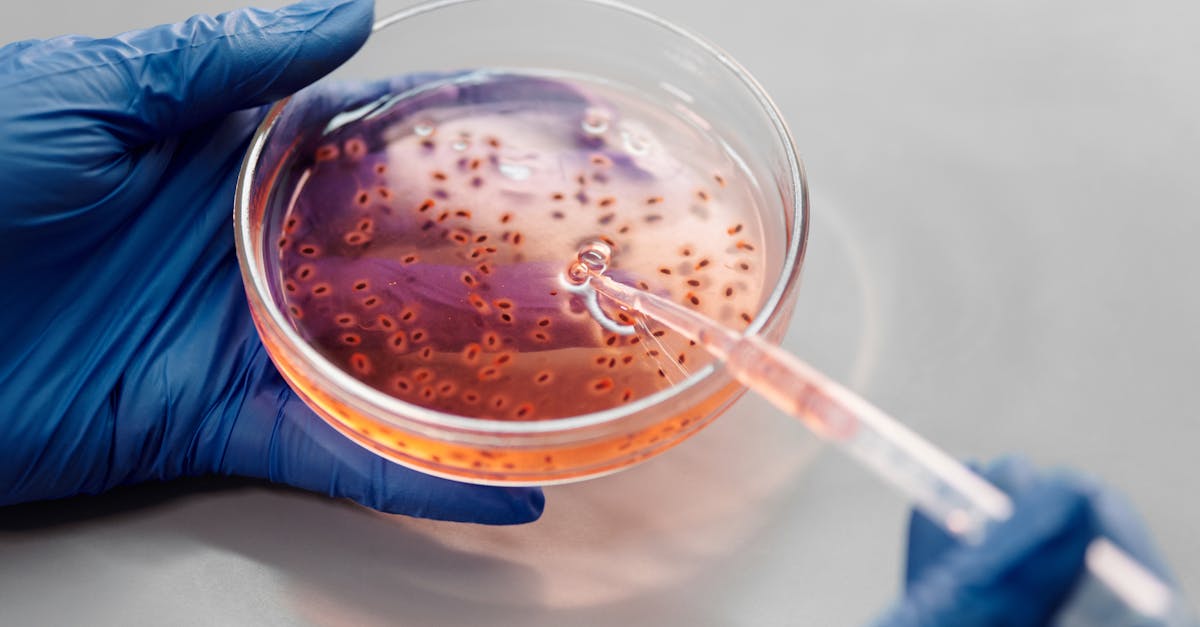
如果保护你免受癌症侵害的疫苗是专门为你量身定制的,那会怎样?这一场景长期以来被认为是科幻小说,如今在2026年正成为现实。因抗击新冠病毒而声名大噪的信使RNA(mRNA)疫苗,正在将自身重新塑造为对抗肿瘤的精准武器。首批临床结果令人震惊,科学界已在谈论治疗最具侵袭性癌症方式的一场革命。
从新冠到癌症:mRNA如何改变靶点
mRNA技术在2020年被推向聚光灯下——彼时BioNTech和Moderna以创纪录的速度开发出了抗SARS-CoV-2疫苗。但在这一壮举背后,隐藏着一个更为古老的项目:利用mRNA教导免疫系统识别并摧毁癌细胞。
其原理十分巧妙。每个肿瘤都携带独特的基因突变,如同分子层面的指纹。个性化mRNA疫苗正是利用了这一特殊性:研究人员从患者肿瘤活检样本中识别出特定突变,然后制造出能够编码这些靶点的定制疫苗。注射后,疫苗指导患者的细胞产生肿瘤蛋白片段,触发有针对性的强效免疫反应。
改变局势的临床结果
2026年,多项II期临床试验正在取得显著成果。Moderna的mRNA-4157(V940)项目与帕博利珠单抗(一种免疫治疗药物)联合使用,在晚期黑色素瘤患者中显示出复发风险的显著降低。监管提交文件有望于今年出炉,这可能使其成为首个获批的治疗性癌症疫苗。
BioNTech方面的结果同样令人鼓舞。其候选疫苗BNT122在三阴性乳腺癌患者(最具侵袭性的乳腺癌类型之一)中进行了测试,产生了强效而持久的免疫反应,在接种后数年内持续存在。肿瘤特异性T淋巴细胞在治疗结束后仍长期保持活跃,表明对复发具有长期保护作用。
胰腺癌的临床试验也在进行中——这是最难治疗的癌症之一,五年生存率不足10%。纽约纪念斯隆-凯特琳癌症中心报告称,个性化mRNA疫苗在一组患者中诱导了持续的免疫活性,为此前治疗选择极为有限的领域带来了希望。
人工智能服务于精准医疗
2026年这一进展之所以成为可能,是分子生物学与人工智能融合的结果。AI算法现在能在数小时内分析肿瘤基因组,识别出最有可能触发有效免疫反应的突变。这一步骤被称为新抗原发现,曾经是一个漫长而不确定的过程。如今,AI使得在活检后不到六周内设计出个性化疫苗成为可能。
递送系统也取得了进展。新一代脂质纳米颗粒能更好地保护mRNA,并更精确地将其导向免疫细胞,在提高疗效的同时减少副作用。整合CRISPR的平台甚至允许通过编辑患者T细胞中的某些基因来优化免疫反应。
超过60种候选疫苗处于临床开发阶段
全球mRNA癌症疫苗管线目前已超过60种处于临床开发阶段的候选疫苗。Moderna、BioNTech、CureVac,以及Gritstone bio和Nuvation Bio等新兴参与者正在大力投资这一领域。研究靶点多样:黑色素瘤、结直肠癌、非小细胞肺癌、胶质母细胞瘤、胰腺癌和乳腺癌。
首批商业批准预计将于2029年前到来,但最先进的项目可能早在2027年就能获得加速授权。风险巨大:与化疗等标准治疗不同,个性化mRNA疫苗只攻击恶性细胞,保护健康组织,大幅降低治疗毒性。
仍需克服的挑战
尽管充满热情,重大障碍依然存在。个性化疫苗的生产成本仍然高昂——每一剂都是为单个患者定制的独特产品。即便在AI的帮助下缩短了生产周期,对于每周都至关重要的快速进展型癌症而言,时间问题仍是一大难题。
研究经费问题同样至关重要。正如《科学美国人》近期一篇文章所指出的,美国联邦机构的预算削减威胁着临床试验的推进速度,尽管此时的研究结果从未如此令人振奋。在欧洲,公共和私人资金目前看来更为稳定,制药行业与大学医院中心之间保持着积极的合作。
最后,患者之间免疫反应的差异性仍是一项挑战。并非所有机体对疫苗的反应都一致,研究人员正致力于识别预测性生物标志物,以便更好地筛选出从治疗中获益最多的患者。
迈向抗癌新时代
个性化mRNA疫苗所代表的远不止一项技术进步:它们象征着医学领域的范式转变。有史以来第一次,治疗方案不再由癌症类型决定,而是由每位患者独特的分子特征决定。这种方法通常被称为精准肿瘤学,可能将癌症从一种常常致命的疾病转变为一种可以长期管理的慢性病。
随着首批治疗性疫苗即将进入市场,我们每个人都面临一个问题:我们准备好进入真正个性化医疗时代了吗?2026年的进展表明答案是肯定的——而最好的时代还在前方。

 Chinese
Chinese  French
French  English
English  Spanish
Spanish  Japanese
Japanese  Korean
Korean  Hindi
Hindi  German
German  Norwegian
Norwegian